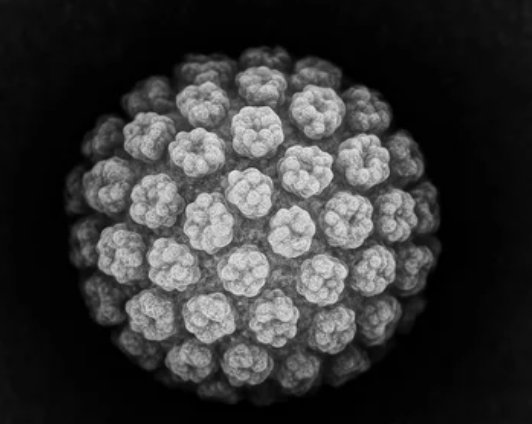
What is HPV
Il Papillomavirus Umano (HPV, Human Papilloma Virus) è un virus a DNA a doppio filamento appartenente alla famiglia Papillomaviridae, privo di involucro lipidico, con spiccato tropismo per le cellule epiteliali della cute e delle mucose. Esistono oltre 200 genotipi classificati, di cui una quarantina in grado di infettare l'epitelio del tratto genitale inferiore. L'HPV è il virus a trasmissione sessuale più frequente al mondo: si stima che circa l'80% delle persone sessualmente attive contragga l'infezione nel corso della vita.
Il virus penetra nell'organismo attraverso microlesioni dell'epitelio ed è in grado di infettare sia la cute cheratinizzata — dove può causare verruche volgari, plantari e piane — sia le mucose non cheratinizzate del tratto anogenitale e dell'orofaringe. In questi ultimi distretti l'infezione assume il maggiore rilievo clinico oncologico.
Nota epidemiologica. In Italia, l'HPV è responsabile di circa 2.400 nuovi casi di carcinoma della cervice uterina l'anno. I genotipi 16 e 18, classificati ad alto rischio oncogeno, causano oltre il 70% di tali tumori. La prevenzione mediante vaccinazione e screening organizzato ha ridotto significativamente l'incidenza nei Paesi con elevata copertura vaccinale.
Transmission and natural history of infection
L'HPV si trasmette prevalentemente attraverso il contatto diretto cute-mucosa durante i rapporti sessuali — vaginali, anali e orali — con un partner infetto. L'utilizzo del preservativo riduce significativamente il rischio di trasmissione, ma non lo elimina completamente, poiché il virus può essere presente su aree non coperte dal dispositivo. Una ulteriore modalità di trasmissione, meno frequente, è quella verticale madre-neonato durante il parto, con possibile insorgenza di papillomatosi laringea ricorrente nel bambino.
La grande maggioranza delle infezioni da HPV — circa l'80-90% — è transitoria: il sistema immunitario dell'ospite è in grado di eliminare il virus spontaneamente entro 1-2 anni. Una quota minoritaria di individui non riesce a eliminare l'infezione, che persiste e può progredire verso lesioni precancerose e, nel tempo, verso un carcinoma invasivo. Il rischio di persistenza e di progressione è significativamente maggiore per i genotipi ad alto rischio oncogeno.
HPV genotypes: low and high risk
In base al loro potenziale oncogeno, i genotipi di HPV vengono suddivisi in due grandi categorie:
- ● Basso rischio HPV 6 e 11: responsabili di condilomi acuminati genitali e di verruche cutanee benigne. Non sono associati al rischio di cancro cervicale.
- ● Alto rischio HPV 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68: possono causare lesioni intraepiteliali della cervice (CIN), dell'ano, della vagina, della vulva e dell'orofaringe, con rischio di progressione a carcinoma invasivo in caso di infezione persistente.
I genotipi 16 e 18 sono di gran lunga i più pericolosi: HPV 16 è il principale agente causale del carcinoma squamoso della cervice, responsabile da solo di oltre il 60% dei tumori cervicali, mentre HPV 18 — associato soprattutto all'adenocarcinoma endocervicale — è implicato in circa il 20% dei casi. Entrambi sono inclusi in tutti i vaccini anti-HPV oggi disponibili.
È importante sottolineare che i genotipi in grado di indurre lesioni precancerose e tumori non causano verruche o condilomi: le due categorie di virus sono distinte e non sovrapposte nella loro azione patogena.
Genital warts
Il condiloma acuminato è la più comune manifestazione clinica delle infezioni da HPV a basso rischio (genotipi 6 e 11) a carico della regione anogenitale. In Italia è la malattia sessualmente trasmissibile più diagnosticata, con una prevalenza stimata di circa l'1% degli adulti sessualmente attivi. Il picco di incidenza si colloca tra i 19 e i 25 anni.
Le lesioni si presentano come escrescenze esofitiche di dimensioni variabili — da piccoli rilievi millimetrici fino a formazioni a cavolfiore — localizzate a livello vulvare, vaginale, perianale, penieno o scrotale. L'intervallo tra l'esposizione al virus e la comparsa delle lesioni è mediamente di 2-3 mesi, ma può essere molto più lungo. Le lesioni possono essere asintomatiche o associarsi a prurito, bruciore, sensazione di peso locale.
Treatment of genital warts
Il trattamento dei condilomi acuminati è finalizzato alla rimozione delle lesioni clinicamente evidenti. Le principali modalità disponibili sono:
- Crioterapia con azoto liquido, applicabile in ambito ambulatoriale per lesioni di piccole dimensioni
- Terapia laser CO₂, indicata per lesioni estese o localizzate in sedi difficili (introito vaginale, uretra distale)
- Escissione chirurgica con bisturi o radiofrequenza, per lesioni peduncolate o voluminose
- Applicazione topica di imiquimod o acido tricloroacetico, in regime domiciliare o ambulatoriale
È fondamentale informare la paziente che, pur dopo la rimozione delle lesioni visibili, il DNA virale può persistere nell'epitelio perifocale: i condilomi possono pertanto recidivare. Il partner sessuale deve essere informato e valutato dallo specialista.
- Appearance of growths or skin irregularities in the genital or perianal area
- Itching, burning, or bleeding unrelated to the menstrual cycle
- Abnormal Pap test or HPV DNA test result
- Sexual partner diagnosed with HPV or genital warts
- Failure to undergo screening in the past 3-5 years
Screening: Pap test
Il Pap test (citologia cervico-vaginale) è un esame citologico che analizza le cellule prelevate dalla cervice uterina per identificare alterazioni morfologiche indicative di infezione da HPV, di lesioni intraepiteliali (precancerose) o di carcinoma invasivo. Introdotto negli anni Quaranta del Novecento dal medico greco-americano Georgios Papanikolaou, è tra le procedure di screening oncologico più efficaci nella storia della medicina.
L'esame viene eseguito in ambiente ambulatoriale: il clinico introduce uno speculum in vagina per visualizzare la cervice, quindi preleva cellule dalla zona di trasformazione (giunzione squamo-colonnare) mediante uno spazzolino endocervicale (cytobrush) e una spatola di Ayre. Il materiale viene inviato al laboratorio per analisi citologica convenzionale o in fase liquida (liquid-based cytology).
Bethesda classification of results
La refertazione dei Pap test adotta la classificazione di Bethesda, che distingue:
- NILM Negativo per lesioni intraepiteliali: esame normale, nessuna alterazione cellulare rilevata.
- ASC-US Atipia delle cellule squamose di significato incerto: alterazioni lievi di interpretazione incerta; richiede integrazione con HPV test di riflessione.
- LSIL Lesione intraepiteliale squamosa di basso grado: alterazioni compatibili con infezione da HPV attiva; nella maggior parte dei casi regredisce spontaneamente.
- HSIL Lesione intraepiteliale squamosa di alto grado: alterazioni precancerose significative che richiedono colposcopia urgente.
- Carcinoma invasivo: diagnosi di carcinoma già manifesto; richiede presa in carico oncologica immediata.
Screening recommendations
- Donne 21–29 anni: Pap test ogni 3 anni
- Donne 30–65 anni: co-test (Pap test + HPV DNA test) ogni 5 anni, oppure solo Pap test ogni 3 anni
- Donne over 65 anni: possibile sospensione dello screening dopo tre Pap test consecutivi negativi o due co-test negativi
- Donne immunodepresse, HIV-positive o con storia di lesioni cervicali: protocolli di sorveglianza individualizzati
Screening: HPV DNA test
L'HPV DNA test è un esame molecolare che ricerca il DNA di genotipi di HPV ad alto rischio oncogeno nelle cellule cervicali. Il prelievo cellulare avviene con le stesse modalità del Pap test. Il test è più sensibile del solo Pap test nell'identificare le lesioni CIN 2+ e consente intervalli di screening più lunghi.
In Italia, le linee guida del Ministero della Salute e del Piano Nazionale per la Prevenzione raccomandano l'HPV DNA test come test di screening primario nelle donne tra 30 e 65 anni, con un intervallo di 5 anni in caso di negatività. La refertazione distingue tra negatività, positività generica ad alto rischio e positività per i genotipi 16/18 (a maggiore rischio oncogeno, con invio diretto a colposcopia indipendentemente dal Pap test).
Validazione dei test HPV. Non tutti i test HPV disponibili sul mercato sono stati validati in studi clinici per l'uso nello screening organizzato. Il GISCI (Gruppo Italiano Screening del Cervicocarcinoma) pubblica e aggiorna periodicamente l'elenco dei test validati raccomandati: è fondamentale che i laboratori utilizzino esclusivamente test inclusi in tale lista.
Colposcopy
La colposcopia è un esame di secondo livello indicato in caso di Pap test anomalo (ASC-US con HPV positivo, LSIL, HSIL, AGC) o di HPV DNA test positivo per genotipi ad alto rischio. Consente di esaminare in dettaglio la cervice uterina, la vagina e la vulva mediante un colposcopio — uno strumento ottico binoculare a ingrandimento variabile (6–40×) — collocato a distanza dalla paziente, che rimane in posizione ginecologica standard.
Durante l'esame, il clinico applica soluzioni rivelanti sulla cervice:
- Acido acetico al 3-5%: le aree con epitelio anormale (ricche di proteine nucleari) appaiono bianche (acetowhite), con intensità proporzionale alla gravità della lesione
- Soluzione di Lugol (iodio-joduro di potassio): il glicogeno dell'epitelio squamoso normale si colora in mogano scuro, mentre le aree patologiche rimangono gialle o iodo-negative
In presenza di aree sospette, viene eseguita una biopsia mirata — prelievo di un frammento di tessuto di 3-5 mm — per l'esame istologico definitivo. La procedura è ambulatoriale e ben tollerata; può causare un lieve disagio e minimo sanguinamento post-bioptico. Il referto istologico colposcopico classifica le lesioni come CIN 1, CIN 2 o CIN 3 (o la nomenclatura LAST: LSIL/HSIL), determinando il percorso terapeutico.
HPV vaccination
La vaccinazione contro l'HPV rappresenta la strategia preventiva primaria più efficace disponibile. Attualmente sono disponibili tre vaccini:
- Vaccino bivalente (Cervarix): copre i genotipi 16 e 18
- Vaccino quadrivalente (Gardasil): copre i genotipi 6, 11, 16 e 18
- Vaccino nonavalente (Gardasil 9): copre i genotipi 6, 11, 16, 18, 31, 33, 45, 52 e 58, responsabili di oltre il 90% dei tumori cervicali HPV-correlati
Il Piano Nazionale di Prevenzione Vaccinale italiano raccomanda la vaccinazione per tutte le ragazze e i ragazzi nel dodicesimo anno di vita (coorte 11-12 anni), con schedula a 2 dosi (0-6 mesi). Nelle persone di età superiore ai 15 anni e negli immunodepressi è indicata una schedula a 3 dosi (0-1/2-6 mesi). Il vaccino è offerto gratuitamente dal SSN fino ai 26 anni.
L'efficacia vaccinale è massima quando somministrata prima dell'esposizione al virus, ma il vaccino nonavalente ha dimostrato protezione anche nelle donne fino a 45 anni non precedentemente infettate dai genotipi inclusi. La vaccinazione non sostituisce lo screening: le donne vaccinate devono continuare a sottoporsi al Pap test o all'HPV DNA test secondo i protocolli raccomandati.
L'HPV (Human Papilloma Virus) è un virus a DNA che infetta le cellule epiteliali di cute e mucose. Si trasmette prevalentemente attraverso il contatto diretto durante i rapporti sessuali (vaginali, anali, orali) con un partner infetto. Più raramente, può trasmettersi dalla madre al neonato durante il parto (papillomatosi laringea).
La maggior parte delle infezioni regredisce spontaneamente entro 1-2 anni grazie alla risposta immunitaria dell'ospite. Solo una minoranza di infezioni persiste e può dare luogo a lesioni precancerose, in particolare con i genotipi ad alto rischio oncogeno.
Rif.: [2, 3, 10]
No. Esistono oltre 200 genotipi di HPV, suddivisi in quelli a basso rischio oncogeno (come HPV 6 e 11, responsabili di condilomi e verruche benigne) e quelli ad alto rischio (come HPV 16 e 18, responsabili di oltre il 70% dei tumori della cervice uterina). I genotipi che causano verruche e condilomi non causano tumori, e viceversa.
I tumori HPV-correlati includono il carcinoma della cervice uterina, della vagina, della vulva, dell'ano, del pene e dell'orofaringe. Il rischio di progressione da infezione a tumore è limitato ai genotipi ad alto rischio e si verifica solo in presenza di infezione persistente non eliminata dal sistema immunitario.
Rif.: [1, 3, 4]
I condilomi acuminati sono lesioni benigne dell'area anogenitale causate dai genotipi HPV 6 e 11. Si presentano come escrescenze di varie dimensioni — spesso paragonabili a piccoli cavolfiori — e possono localizzarsi sulla vulva, in vagina, a livello perianale, sul pene o sullo scroto. Sono la malattia sessualmente trasmissibile più diagnosticata in Italia.
Il trattamento prevede la rimozione delle lesioni visibili mediante crioterapia, laser CO₂, escissione chirurgica o terapia topica (imiquimod, acido tricloroacetico). È importante ricordare che il DNA virale può persistere nell'epitelio circostante anche dopo la rimozione, con possibile recidiva delle lesioni. Il partner sessuale deve essere valutato da uno specialista.
Rif.: [3, 10]
Le linee guida internazionali raccomandano: Pap test ogni 3 anni per le donne tra 21 e 29 anni; co-test (Pap test + HPV DNA test) ogni 5 anni o Pap test ogni 3 anni per le donne tra 30 e 65 anni. Dopo i 65 anni, lo screening può essere interrotto se i precedenti esami sono stati regolarmente negativi.
Donne con fattori di rischio particolari — immunodepressione, infezione da HIV, storia di CIN 2+ o di carcinoma in situ — necessitano di protocolli di sorveglianza più intensivi, da concordare individualmente con lo specialista.
Rif.: [7, 8]
Un risultato anomalo al Pap test non significa necessariamente la presenza di un tumore. Indica la presenza di alterazioni cellulari che richiedono un approfondimento diagnostico. In base alla categoria Bethesda (ASC-US, LSIL, HSIL), lo specialista indicherà il percorso più appropriato: un HPV test di riflessione, un controllo citologico a breve termine o una colposcopia.
La maggior parte delle anomalie di basso grado (ASC-US, LSIL) regredisce spontaneamente. Le lesioni di alto grado (HSIL) richiedono invece una valutazione colposcopica urgente e, se confermata istologicamente, un trattamento escissionale (LEEP/conizzazione).
Rif.: [7, 8]
L'HPV DNA test è un esame molecolare che rileva il DNA di genotipi di HPV ad alto rischio oncogeno nelle cellule cervicali. Il prelievo avviene con le stesse modalità del Pap test. Ha una maggiore sensibilità rispetto al solo Pap test nell'identificare le lesioni CIN 2+ e consente intervalli di screening più lunghi in caso di negatività.
In Italia, le linee guida raccomandano l'HPV test come test di screening primario nelle donne tra 30 e 65 anni. Si raccomanda di utilizzare solo test validati in studi clinici, secondo le raccomandazioni del GISCI. Un risultato positivo per HPV 16/18 comporta l'invio diretto a colposcopia, indipendentemente dall'esito del Pap test.
Rif.: [7, 8]
La colposcopia è un esame di secondo livello che consente di esaminare in dettaglio la cervice uterina e la vagina mediante uno strumento ottico a ingrandimento (colposcopio). Viene indicata in presenza di Pap test anomalo o di HPV test positivo per genotipi ad alto rischio. L'applicazione di soluzioni rivelanti (acido acetico, soluzione di Lugol) permette di identificare le aree sospette per lesioni intraepiteliali.
In presenza di aree acetowhite o iodo-negative significative, viene eseguita una biopsia mirata per la diagnosi istologica definitiva. La procedura è ambulatoriale, generalmente ben tollerata, e dura pochi minuti. Il referto istologico determina il successivo percorso terapeutico (sorveglianza, LEEP, conizzazione).
Rif.: [3, 8]
Sì, sebbene l'efficacia sia massima quando la vaccinazione avviene prima dell'esordio dell'attività sessuale (età 9-14 anni). Il vaccino nonavalente ha dimostrato efficacia nella prevenzione delle lesioni correlate ai genotipi inclusi anche nelle donne fino a 45 anni che non siano già state infettate da quegli stessi genotipi al momento della vaccinazione.
La decisione di vaccinare un adulto non precedentemente immunizzato deve essere valutata individualmente con lo specialista, tenendo conto dell'anamnesi infettivologica e dell'esito degli esami di screening. La vaccinazione non sostituisce in nessun caso il controllo ginecologico e lo screening cervicale periodico.
Rif.: [5, 6, 9]
I ● genotipi a basso rischio (principalmente HPV 6 e 11) causano quasi la totalità dei condilomi genitali e delle verruche anogenitali, ma non sono associati al rischio di cancro cervicale. Le lesioni che inducono sono benigne e nella maggior parte dei casi non richiedono trattamento urgente.
I ● genotipi ad alto rischio (in primis HPV 16 e 18) possono invece indurre lesioni intraepiteliali (CIN) che, in caso di persistenza dell'infezione, evolvono verso il carcinoma invasivo. HPV-16 è responsabile di oltre il 60% dei tumori cervicali, HPV-18 di circa il 20%. Sul piano clinico, un test positivo per HPV-16 o HPV-18 impone l'invio diretto a colposcopia, indipendentemente dall'esito del Pap test.
Rif.: [11, 12]
Il preservativo offre una protezione parziale, non totale. L'uso corretto e costante è associato a una riduzione di circa il 70% dell'incidenza di infezioni da HPV oncogeni nelle donne e di circa il 50% negli uomini. La protezione è incompleta perché l'HPV può infettare aree della cute anogenitale non coperte dal dispositivo.
Nonostante questo limite, il preservativo rimane uno strumento preventivo importante: può accelerare la clearance virale e ridurre il rischio di condilomi e di neoplasia cervicale. Il suo utilizzo è raccomandato in combinazione — non in sostituzione — alla vaccinazione e allo screening periodico.
Rif.: [13, 14, 15]
Nella maggior parte dei casi il sistema immunitario elimina l'infezione spontaneamente. Circa il 70% delle nuove infezioni si risolve entro 1 anno, e circa il 90% entro 2 anni. La durata mediana dell'infezione è di circa 8 mesi. Studi recenti con alta risoluzione temporale indicano che dopo la fase attiva l'infezione raggiunge un plateau di durata media 13-20 mesi, seguito da una rapida fase di clearance.
Le infezioni da genotipi ad alto rischio tendono a persistere più a lungo rispetto a quelle da genotipi a basso rischio. La mancata clearance entro 12-24 mesi — specialmente con HPV-16 o HPV-18 — aumenta significativamente il rischio di sviluppare lesioni precancerose e richiede uno stretto follow-up colposcopico.
Rif.: [14, 16, 17]
Le principali linee guida internazionali (CDC 2021) affermano chiaramente che non è raccomandato il test HPV per i partner maschili di donne HPV-positive. È probabile che i partner condividano già l'infezione; tuttavia, non esistono test HPV validati per lo screening di routine negli uomini, e il loro esito non modifica la gestione clinica della coppia.
In caso di condilomi visibili, il partner deve essere valutato dallo specialista per una diagnosi clinica. Alcuni studi recenti suggeriscono che i partner di donne con lesioni cervicali ad alto grado (HSIL) potrebbero beneficiare di una peniscopia, ma questa non è ancora una raccomandazione standard nelle linee guida consolidate. La scelta migliore resta la vaccinazione del partner non precedentemente immunizzato.
Rif.: [15, 18, 19]
È una situazione comune, che interessa circa il 4% delle donne di età ≥30 anni: indica la presenza del DNA virale nelle cellule cervicali senza alterazioni citologiche ancora visibili al microscopio. L'HPV DNA test ha una sensibilità superiore al 90% nel rilevare lesioni precancerose, mentre la sola citologia raggiunge il 50-70%. Il virus è quindi presente, ma le cellule non hanno ancora sviluppato le modificazioni morfologiche caratteristiche.
Il rischio di lesione CIN3+ a 12 mesi in questa situazione è stimato tra lo 0,8% e il 4,1%. La gestione prevede tipicamente un controllo a 1 anno con HPV test o co-test, oppure una genotipizzazione immediata per HPV-16/18: se positiva, è indicata la colposcopia senza attendere l'anno di follow-up.
Rif.: [11, 20, 21]
Non esiste un'indicazione assoluta alla rimozione immediata in tutti i casi: i condilomi possono regredire spontaneamente entro meno di un anno nel 30-40% dei casi. Il trattamento è tuttavia indicato quando le lesioni causano sintomi significativi (dolore, prurito, sanguinamento), quando determinano un rilevante disagio psicologico o estetico, quando sono di grandi dimensioni tali da poter ostruire il canale del parto, o quando la paziente ne fa esplicita richiesta.
Le opzioni terapeutiche si suddividono in: trattamenti applicati dalla paziente (imiquimod crema 5%, podofilox, sinecatechine) e trattamenti ambulatoriali eseguiti dallo specialista (crioterapia, acido tricloroacetico, escissione chirurgica o laser CO₂). La scelta dipende da numero, dimensione e localizzazione delle lesioni, nonché dalla preferenza e dalla compliance della paziente.
Rif.: [15, 22]
Dipende da quante dosi sono state ricevute e a quale età. Se la serie vaccinale è stata completata regolarmente, non è previsto alcun richiamo di routine: gli studi a lungo termine dimostrano una protezione duratura contro i genotipi HPV 16 e 18 per almeno 12 anni dalla vaccinazione, senza indicazione per dosi aggiuntive.
Se invece la serie non è stata completata, il vaccino nonavalente può essere utilizzato per continuarla o completarla, senza ricominciare dall'inizio. Di seguito le indicazioni precise delle principali autorità scientifiche.
- Serie incompleta (es. solo 2 dosi ricevute prima dei 15 anni): è sufficiente una sola dose aggiuntiva del vaccino nonavalente per completare la protezione. La serie non va ricominciata da capo, indipendentemente da quanto tempo è trascorso dall'ultima somministrazione.
- Vaccinazione iniziata a 15 anni o più: la serie completa prevede 3 dosi totali. Chi ha ricevuto 2 dosi necessita quindi di 1 sola dose di completamento.
- Serie già completata con 3 dosi (quadrivalente o bivalente): la rivaccinazione di routine con il nonavalente non è raccomandata. Il vaccino precedente si è dimostrato altamente efficace; la dose aggiuntiva apporta un beneficio marginale nella popolazione già immunizzata.
- Ritardi tra le dosi: la serie vaccinale non deve mai essere riavviata in caso di ritardo nella somministrazione di una dose, qualunque sia la durata dell'intervallo.
In sintesi: il vaccino nonavalente è interscambiabile con il quadrivalente per continuare o completare una serie vaccinale già iniziata; non è invece necessario un booster per chi ha completato correttamente la schedula originale.
Rif.: [27, 28, 12]
Per informazioni sulla visita ginecologica e il percorso diagnostico iniziale, inclusi Pap test, HPV test e consulenza ginecologica di base, visita il portale dedicato alla ginecologia clinica.
iltuoginecologo.it → Ginecologia clinica
Link istituzionali:
Ministero della Salute ·
Le 100 domande sull'HPV — GISCI
Request a Specialist Consultation
For a personalized HPV risk assessment, an individual screening pathway, or a vaccination consultation, Prof. Di Donato offers specialist consultations in Rome.
Book a Consultation →